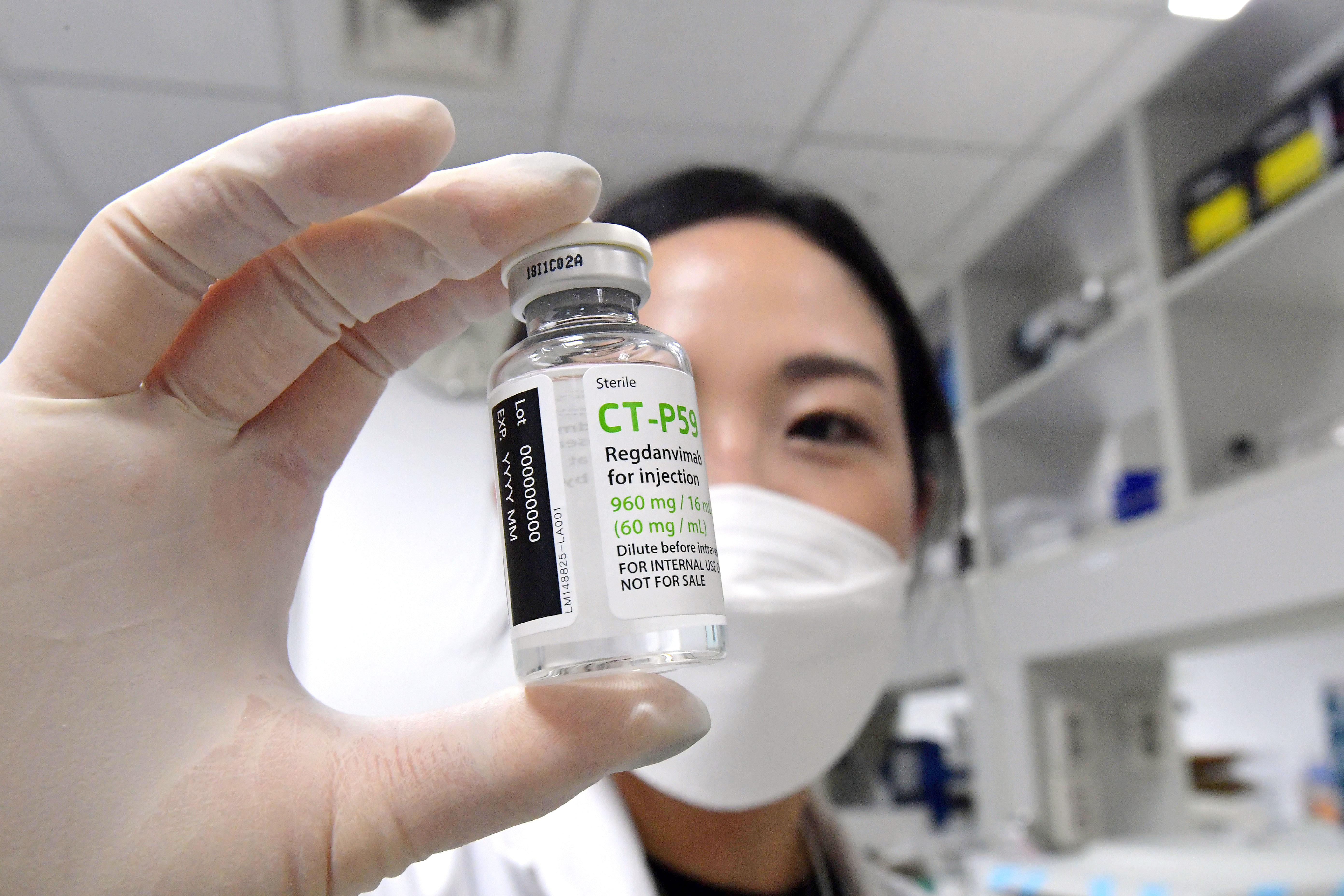
▲南韓藥廠賽特瑞恩研發新冠抗體治療藥物「Regkirona」CT-P59。(圖/達志影像)
記者羅翊宬/編譯
南韓國內生技藥廠賽特瑞恩所研發的新冠病毒抗體治療藥物「Regkirona」(렉키로나,編碼為CT-P59)繼今年9月正式通過該國食藥處正式品項許可後,日前再度傳來捷報,歐洲藥品管理局(以下稱EMA)旗下的人體用藥委員會(以下稱CHMP)建議批准使用,預估未來1至2個月內可正式通過歐盟核准使用。
根據《韓聯社》報導,CHMP於當地時間11日首度建議批准使用2款新冠病毒抗體治療藥物,包括南韓生技藥廠賽特瑞恩所研發的Regkirona,以及美國雷傑納隆藥廠(再生元製藥,Regeneron Pharmaceuticals)所研發的Ronapreve,這2款藥物若最終通過歐盟批准使用,將優先投入疫情急速擴散的歐洲國家使用,而Regkirona也將成為南韓國內第1個獲歐盟批准使用的國產新冠抗體新型藥物。
生技製藥業者們透露,一旦藥品獲得CHMP建議批准使用,其實就代表著未來歐盟將會正式通過批准使用。Regkirona為靜脈注射型藥物,適用該款藥物的對象為無需供應氧氣、卻有著高度機率病情惡化至重症的18歲以上患者,建議使用方法為將該款藥物注射進靜脈約60分鐘。
至於美國雷傑納隆藥廠所研發的Ronapreve,CHMP則建議批准使用於感染新冠肺炎、且有高風險惡化至重症的12歲以上青少年與成人(體重至少40公斤以上),CHMP還建議該款藥物可用於預防12歲以上民眾感染新冠肺炎。
報導指出,南韓的賽特瑞恩與美國的其實早就於今年10月初向EMA提出上市許可申請(MAA),而EMA則表示最晚2個月以內發表最終意見。
據悉,被視為南韓「國產1號」的新冠抗體治療藥物Regkirona已於今年7、8月分別通過印尼與巴西食藥當局的緊急批准使用,而在南韓當局於9月通過後,目前南韓國內已有127間醫療院所、共計2萬1366名患者使用該款藥物;而業者更透露,目前正加快速度研發同款藥物的「吸入型」藥物,透過支氣管黏膜項體內傳遞抗體,可用於居家治療,目前澳洲正進行臨床實驗。
►對抗變種病毒露曙光!南韓藥廠研發「雞尾酒抗體藥」 9月進行臨床
►南韓研發新冠治療藥劑!老鼠實驗證實:「對Delta變種病毒有效」
★《宇宙人外信》:時事閒聊學英文★









讀者迴響